
Alexandre Barros
Até o fim do século XIX e início do século XX, cristalógrafos e mineralogistas haviam acumulado uma série de informações a respeito dos cristais pelos ângulos formados pelas faces, composição química e propriedades mecânicas, mas pouco havia sido levantado sobre o interior da estrutura atômica. Com o surgimento da mecânica quântica, no início do século XX, explicando os fenômenos que ocorrem em escala atômica, abriu-se para esses pesquisadores a perspectiva de interpretar a estrutura dos materiais que até então era somente fruto de especulações.
Os átomos do século XIX eram considerados esferas perfeitas, agrupadas lado a lado unidas pelas ligações químicas que se assemelhavam a molas. Assim, em 1848, o cristalógrafo francês Bravais determinou matematicamente que esferas poderiam ser arranjadas no espaço através de no máximo 14 arranjos, estes arranjos ficaram conhecidos como os 14 sólidos de Bravais.
Entretanto, a experiência de Rutherford, mostrou que o átomo é um "imenso" vazio, com a massa concentrada no núcleo, isso poderia ter causado um certo alvoroço, mas sempre sobram as forças interatômicas, que acabam por deixar os átomos nos seus devidos lugares. Assim, para o cristalografo os átomos poderiam continuar sendo esferas perfeitas.
Mas como provar que esses arranjos formavam as estruturas cristalinas dos materiais ? Para que possamos observar algo, o meio que usaremos para captar dados tem que ser menor que o objeto estudado, se o meio for maior que o objeto esse não terá sensibilidade par captar seus detalhes, como se usando as mãos e com os olhos fechados, quiséssemos descrever o formato de um grão de areia . Assim, para observarmos átomos não poderíamos usar a luz visível, já que os diâmetros atômicos são da ordem de angstrons (10-10 m), com isso, estruturas cristalinas como a cúbica do NaCl (sal de cozinha), tem 5,64 angstrons de face, já a luz visível, apresenta uma faixa de comprimento de onda de 4000 (violeta) até 7000 (vermelho) angstrons. Ou seja, o menor comprimento de onda da luz visivel é cerca de 800 vezes maior que uma aresta da estrutura cúbica do sal de cozinha. Assim, o uso de luz visível para uma observação direta da estrutura cristalina está completamente descartada.
 |
|
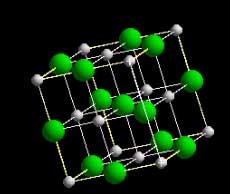
Estrutura
cúbica do sal de cozinha, onde as esferas verdes são os atomos de
cloro (Cl-) e as esferas cinzas os átomos de sódio (Na+).
|
Ocorre que em 1895 Roentger descobriu acidentalmente os raios-X, que assim como as luz visível é uma radiação eletromagnética, mas com comprimento de onda na faixa de 0,5 até 2,5 angstrons. Ora, então poderíamos observar os átomos usando os raios-X ? Infelizmente não, isso porque os raios-X possuem alta energia, assim, quando eles atingem um átomo eles acabam interagindo com ele não retornando na forma de imagens, além disso, os átomos não são esferas rígidas, são uma estrutura complexa formada por elétrons, prótons e neutrons. Mas conhecia-se o fenômeno da difração, onde, quando um feixe de luz monocromático (apenas um comprimento de onda) passava por duas fendas formava franjas brilhantes intercaladas por escuras num anteparo. Se conhecêssemos os espaçamento das franjas brilhantes e o comprimento de onda poderíamos dizer a distância entre as duas fendas.
Foi então que em 1912 o físico alemão von Laue, sugeriu que se os átomos apresentam uma estrutura cristalina, átomos organizados de forma a apresentem periodicidade ao longo do espaço, e que se os raios-X eram ondas eletromagnéticas com comprimento de onda menor que os espaços interatômicos, então os núcleos atômicos que concentram a massa dos átomos poderiam difratar os raios-X, formando franjas de difração. Quando Laue fez passar um feixe de raios-X por uma amostra monocristalina, e pôs um filme fotográfico após a amostra, o resultado foi que após revelar o filme este apresentava pontos sensibilizados pelos raios-X difratados.
As experiências de Laue despertaram grande interesse nos físicos ingleses, W. H. Bragg e seu filho W. L. Bragg, que formularam, ainda em 1912, uma equação extremamente simples para prever os ângulos onde seriam encontrados os picos de intensidade máxima de difração. Assim, conhecendo-se as distâncias interatômicas, poderiam ser resolvidas os problemas envolvidos na determinação da estrutura cristalina. Dessa forma, os Bragg determinaram sua primeira estrutura, a do NaCl. Transformando a difração de raios-X na primeira ferramenta eficiente para determinar a estrutura atômica dos materiais, fazendo com que a técnica obtivesse rapidamente grande popularidade entre os institutos de pesquisa.
Entre as décadas de 1920 e 1930, a literatura foi inundada por estruturas cristalinas determinadas por difração de raios-X. Todo mineralogista ou cristalografo da época tinha por obrigação determinar a estrutura cristalina de algum composto, mineral ou metal. A difração de raios-X também provocou surpresa ao demonstrar a estrutura amorfa do vidro, onde este na realidade é um líquido super-resfriado com viscosidade tendendo ao infinito, e também foi a principal ferramenta usada por Watson e Crick, em 1953, para propor a estrutura em dupla hélice do DNA.
 |
|
Padrão
de difração de raios-X do DNA.
|
Mas e a mecânica quântica ? Para falar a verdade, os princípios da mecânica quântica pouco se aplicam às primeiras fases da difração de raios-X. Mas a explicação de como são gerados os raios-X é fruto da mecânica quântica. Além disso, para que a técnica seja eficiente é necessário gerar um raio-X monocromado e, nesse caso, entram os princípios da geração da radiação característica, que é fruto da explicação de Bohr para a lei de Rydberg.
Em 1925, Louis de Broglie, havia explicado as órbitas dos elétrons como se esses se comportassem como uma onda, criando o conceito de que a matéria poderia apresentar a dualidade onda/partícula. Consequentemente, em 1927, Davisson e Germer, simultaneamente com Thompson e Reid, provaram a natureza ondulatória do elétron ao realizar a clássica experiência de difração e, em 1936, Mitchell e Powers provaram o mesmo para o nêutron.
A partir dessa comprovação surgiu a idéia de usar os elétrons para gerar imagens, pois estes possuem cargas elétricas, portanto, poderiam ter sua trajetória alterada por lentes magnéticas. Dessa forma, em 1932, Knoll e Ruska criaram o primeiro microscópio eletrônico, que era do tipo transmissão.
Nesse tipo de microscópio o feixe de elétrons deve atravessar uma amostra muito fina, ou pelo menos que seja "transparente" a elétrons. As interações do feixe com os átomos da amostra gera uma imagem numa placa pintada com uma tinta fluorescente. Esse tipo de microscópio causou um grande entusiasmo para os cientistas de materiais da época, pois pôde-se criar uma figura de difração de uma fase observada no material e, consequentemente, determinar a estrutura cristalina de cada fase constituinte do material. O problema é que como o feixe atravessa a amostra, as imagens geradas são somente em duas dimensões, referindo-se exclusivamente ao interior do material, não sendo possível observar a superfície das amostras.
Para superar esse problema, o próprio Knoll, em 1935, gerou a primeira imagem por varredura de elétrons. Por esse método, o feixe não fica fixo, mas varre a seção da amostra que se quer observar através de uma sequência de linhas. Os elétrons que são espalhados pela superfície, são captados por sensores que geram a imagem como numa transmissão de televisão, ou seja, ao contrário do microscópio de transmissão, no de varredura a imagem tem que ser processada e não gerada diretamente. O primeiro trabalho propondo esse método foi publicado em 1938 pelo alemão von Ardenne, mas as pesquisas de Ardenne acabaram sendo tragicamente interrompidas, quando seu primeiro protótipo foi destruído por um bombardeio em 1944. Assim, o primeiro microscópio eletrônico de varredura acabou surgindo somente em 1947, na Universidade de Cambridge, construído por Charles Oatley.
 |
|
O
primeiro microscópio eletrônico de varredura na Universidade de
Cambridge, e a primeira imagem (amostra de alumínio atacada).
|
A grande importância que esses microscópios apresentam na caracterização dos materiais é indiscutível, não somente por poder observar estruturas que estavam inacessíveis pelo microscópio ótico, mas pela grande vantagem de que, como os elétrons são uma radiação ionizante, o choque dos elétrons de alta energia contra os átomos da amostra resulta na geração de uma série de sinais. Entre esses sinais temos os raios-X, que saem em comprimentos de onda característicos de cada espécie atômica. Dessa forma os microscópios eletrônicos podem gerar análises químicas de cada fase simultaneamente à geração das imagens. Nos microscópios de transmissão pode-se ainda realizar a difração de elétrons de cada fase, determinando a estrutura cristalina.
Outra grande vantagem sobre os microscópios óticos é que o microscópio eletrônico de varredura, apresenta a propriedade de ter uma grande distância focal, ou seja, pode-se por em foco imagens de uma superfície muito irregular. A perspectiva que essa propriedade abriu para a interpretação de fraturas foi imensa. A partir desse momento, poderíamos observar o aspecto de peças fraturadas e assim determinar tanto o motivo da quebra do material, como o comportamento dessa trica durante a propagação.
Mas, e para um engenheiro que esteja estudando a deformação de um metal? Onde entraria a Física Quântica? Na verdade, para a deformação de um material dúctil, como alguns metais, os átomos podem perfeitamente ser esferas rígidas, onde o efeito da deformação ocorre pelo escorregamento de uma esfera sobre a outra. Mas para que uma esfera possa escorregar ela precisa se desligar daquela a qual tinha sua ligação original. Assim, o cálculo de energia de ligação química que a mecânica quântica gerou, assim como a explicação detalhada de como se comportavam as ligações metálicas e covalentes, foi de grande importância para prever o comportamento mecânico de metais e cerâmicas.
Mas, em 1928, Orowan, na época um jovem estudante de metalurgia, ao iniciar as experiências para seu trabalho de formatura, submetendo uma amostra monocristalina de zinco metálico a um ensaio de tração, observou que a energia necessária para fraturar o material era muito menor do que a prevista pelas energias de ligação. Nessa época acreditava-se que um cristal apresentava uma estrutura perfeita, com átomos organizados lado a lado sem nenhuma falha. Portanto, se conhecêssemos as energias de ligação, a estrutura cristalina e quantos átomos temos no corpo de prova poderíamos dizer qual seria a força necessária para fraturar a amostra.
Com isso, surgiram uma série de hipóteses de defeitos na estrutura cristalina dos materiais. Em 1934, Orowan, simultaneamente a Taylor, propôs que a estrutura cristalina não era perfeita, que ao longo dos planos atômicos empilhados poderiam haver falhas. Essas falhas foram chamadas de discordâncias ou deslocações. Na época a idéia não foi muito aceita, pois a difração de raios-X não era sensível o suficiente para detectar essas falhas e não existiam instrumentos de observação direta dos planos cristalinos. Mas, a teoria da discordância se adaptava muito bem aos resultados obtidos na prática para a deformação dos materiais. Finalmente em 1956, Bollmmann, Hirsch, Horne e Whelan, observaram, pela primeira vez, uma discordância por um microscópio eletrônico de transmissão. Mas qual a importância desse fato ? O resultado, é que esses defeitos cristalinos regem a deformação dos metais, o empilhamento de defeitos implica no surgimento de uma região onde os átomos perdem suas ligações e que, consequentemente, resulta no surgimento e crescimento de trincas, ao mesmo tempo que o empilhamento dos defeitos provoca o endurecimento dos metais. O conhecimento de como esses defeitos se comportam, durante a deformação, permite determinar o processamento dos metais.
Como exemplo temos o processo de estamparia. A porta do seu automóvel era originalmente uma plana chapa de aço Essa chapa é colocada entre dois moldes que apresentam o formato final da porta. Quando uma prensa impõe uma deformação, pelo fechamento dos dois moldes, temos o produto.
O mais recente produto para a observação da estrutura da matéria são os microscópio de varredura por tunelamento, desenvolvido em 1981 por Binnig e Roher dos laboratórios da IBM de Zurique. Esse instrumento torna quase mentiroso o conceito de que átomos não podem ser observados.
O funcionamento desse microscópio, grosso modo, é semelhante ao dos antigos toca-discos de vinil. No microscópio de tunelamento, uma agulha funciona como sonda varrendo a superfície de uma amostra condutora. Entre a sonda e a amostra é aplicada uma voltagem. Os elétrons da amostra deveriam permanecer nos átomos, mas pela mecânica quântica os elétrons podem "tunelar" da amostra para a sonda gerando uma diminuta corrente elétrica. Quando a sonda percorre paralelamente a superfície da amostra, as variações de corrente elétrica determinam as colinas e vales da superfície. A agulha assim consegue "enxergar" a topografia dos átomos. Para que esse equipamento possa ter uma resolução atômica, a agulha tem que ser tão fina que a espessura da ponta deve ser de um único átomo.
O microscópio de tunelamento consegue gerar imagens somente em amostras condutoras elétricas. Para amostras isolantes, foi desenvolvido em 1986, o microscópio de força atômica. A técnica é semelhante ao microscópio de tunelamento, mas nesse caso não há a geração da corrente de tunelamento. Mas são usadas as forças de repulsão entre os átomos, as mesmas forças que impedem que sua mão atravesse uma parede. Assim, num microscópio de força atômica, a agulha, ao aproximar a eletrosfera do seu último átomo das eletrosferas dos átomos da amostra, sofre a ação de forças de repulsão. A agulha está apoiada sobre uma alavanca onde há um espelho que reflete um feixe de laser, as variações do feixe refletido determinam os movimentos da agulha e consequentemente o relevo da amostra.
Levantar o perfil topológico de amostras, com a possibilidade de atingir resolução atômica, abre a possibilidade de perceber desde a rugosidade e determinar o acabamento superficial, até determinar os primeiros estágios de oxidação de metais. Lógico que se temos um instrumento que possibilita a visualização de átomos, também temos a possibilidade de criar métodos para manipulá-los. Uma brincadeira que passou a existir com o microscópio de tunelamento, foi a de criação de letras com átomos, como criar o nome IBM com 35 átomos de xenônio.
Mas as implicações tecnológicas estão sem dúvida na indústria eletrônica, onde os microprocessadores são compostos por transistores impressos em placas de silício metálico. Com a possibilidade de analisar a topografia da impressão desse transistor, pode-se criar métodos para imprimir componentes eletrônicos confiáveis cada vez menores. Não é sem motivo que o microscópio de tunelamento surgiu na IBM.
Enfim, no século XX observamos o surgimento de novos tipos de aços, os polímeros passaram a ser materiais confiáveis e comercialmente viáveis, ligas de alumínio invadiram o mercado e as cerâmicas deixaram de ser meramente um material de decoração. Saímos de um século XIX, onde os materiais se resumiam a aços frágeis usados em construção mecânica, madeiras e pedras para a construção civil. Entramos no século XXI com aços resistentes sem serem frágeis, plásticos que não se deterioram rapidamente se tornando tintas resistentes e o concreto, cujo principal componente é o cimento portland comum, o segundo produto mais consumido pela raça humana perdendo somente para a água.
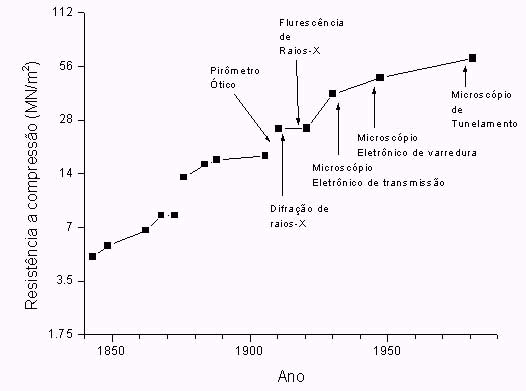
Podemos atualmente levantar a composição química de metais enquanto eles ainda estão fundidos, determinar a temperatura dos processos e assim obter um controle eficiente do produto final, caracterizar a estrutura cristalina dos materiais e assim prever se este será dúctil ou frágil. E todo esse desenvolvimento veio graças aos instrumentos que a mecânica quântica trouxe à ciência dos materiais. Em 150 anos, observamos que o cimento portland comum aumentou a resistência à compressão em 20 vezes, e coincidentemente, o aparecimento de instrumentos que identificam a estrutura da matéria, também resultaram em saltos nas propriedades mecânicas.
 |
|
Evolução
da resistência à compressão do cimento portland comum (amostra com
28 dias de hidratação) ao longo dos anos. Reparar que a escala de
propriedades mecânicas não é linear.
|
As aplicações da mecânica quântica são óbvias na indústria eletrônica, com a criação de componentes como os transistores e os microprocessadores. Mas o desenvolvimento da indústria metal/mecânica, o surgimento de novos materiais, assim como a construção civil, se valeram dos instrumentos que a mecânica quântica forneceu para a análise e caracterização dos materiais. Hoje observamos que os métodos criados pela mecânica quântica se transformaram em instrumentos comuns no ambiente industrial, tanto como controladores de processos como no controle de qualidade, e que o fim da evolução dos métodos atuais, e surgimento de novos ainda está longe de ser atingido.
Alexandre M. Barros é doutor em Engenharia de Materiais pela EPUSP.
Atualizado em 10/05/2001
http://www.comciencia.br
contato@comciencia.br
© 2001
SBPC/Labjor
Brasil